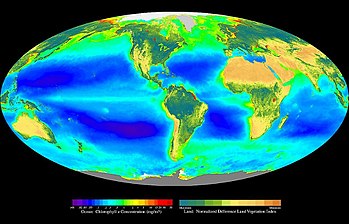
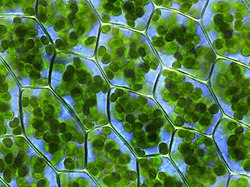
Fotosíntesis oxigénica y anoxigénica.
La
fotosíntesis (del
griego antiguo φῶς-φωτός [
fos-fotós], ‘luz’, y
σύνθεσις [
sýnthesis], ‘composición’, ’síntesis’) es la conversión de materia inorgánica en materia orgánica gracias a la energía que aporta la
luz. En este proceso la
energía lumínica se transforma en
energía química estable, siendo el
adenosín trifosfato (ATP) la primera
molécula en la que queda almacenada esta energía química. Con posterioridad, el
ATP se usa para sintetizar
moléculas orgánicas
de mayor estabilidad. Además, se debe de tener en cuenta que la vida en
nuestro planeta se mantiene fundamentalmente gracias a la fotosíntesis
que realizan las
algas, en el medio acuático, y las plantas, en el medio terrestre, que tienen la capacidad de sintetizar
materia orgánica (imprescindible para la constitución de los
seres vivos) partiendo de la luz y la
materia inorgánica.
De hecho, cada año los organismos fotosintetizadores fijan en forma de
materia orgánica en torno a 100.000 millones de toneladas de
carbono.
1 2
Los
orgánulos citoplasmáticos encargados de la realización de la fotosíntesis son los
cloroplastos, unas estructuras polimorfas y de color verde (esta coloración es debida a la presencia del pigmento
clorofila) propias de las
células vegetales.
En el interior de estos orgánulos se halla una cámara que contiene un
medio interno llamado estroma, que alberga diversos componentes, entre
los que cabe destacar enzimas encargadas de la transformación del
dióxido de carbono en materia orgánica y unos sáculos aplastados denominados
tilacoides
o lamelas, cuya membrana contiene pigmentos fotosintéticos. En términos
medios, una célula foliar tiene entre cincuenta y sesenta cloroplastos
en su interior.
1
Los organismos que tienen la capacidad de llevar a cabo la fotosíntesis son llamados
fotoautótrofos (otra nomenclatura posible es la de
autótrofos, pero se debe tener en cuenta que bajo esta denominación también se engloban aquellas bacterias que realizan la
quimiosíntesis) y fijan el
CO2 atmosférico. En la actualidad se diferencian dos tipos de procesos fotosintéticos, que son la
fotosíntesis oxigénica y la
fotosíntesis anoxigénica. La primera de las modalidades es la propia de las plantas superiores, las algas y las
cianobacterias, donde el dador de electrones es el
agua y, como consecuencia, se desprende
oxígeno. Mientras que la segunda, también conocida con el nombre de fotosíntesis bacteriana, la realizan las
bacterias purpúreas y
verdes del azufre, en las que el dador de electrones es el
sulfuro de hidrógeno, y consecuentemente, el elemento químico liberado no será oxígeno sino
azufre, que puede ser acumulado en el interior de la bacteria, o en su defecto, expulsado al agua.
3
A comienzos del
año 2009, se publicó un artículo en la
revista Nature Geoscience en el que
científicos norteamericanos daban a conocer el hallazgo de pequeños cristales de
hematita (en
Cratón de Pilbara, en el
noroeste de
Australia), un
mineral de
hierro que data de la época del
eón Arcaico,
demostrando la existencia de agua rica en oxígeno y consecuentemente,
de organismos fotosintetizadores capaces de producirlo. Gracias al
estudio realizado, se ha llegado a la conclusión de la existencia de
fotosíntesis oxigénica y de la oxigenación de la atmósfera y de los
océanos hace más de 3.460 millones de años, así como también se deduce
la existencia de un número considerable de organismos capaces de llevar a
cabo la fotosíntesis para oxigenar la masa de agua mencionada, aunque
sólo fuese de manera ocasional.
4 5
Historia del estudio de la fotosíntesis
Desde la Antigua Grecia hasta el siglo XIX
Ya en la
Antigua Grecia, el
filósofo Aristóteles propuso una
hipótesis
que sugería que la luz solar estaba directamente relacionada con el
desarrollo del color verde de las hojas de las plantas, pero esta idea
no trascendió en su época, quedando relegada a un segundo plano. De
hecho, no volvió a ser recuperada hasta el
siglo XVII, cuando el considerado padre de la
fisiología vegetal,
Stephen Hales,
hizo mención a la citada hipótesis aristotélica. Además de retomar este
supuesto, el mismo Hales afirmó que el aire que penetraba por medio de
las hojas en los vegetales, era empleado por éstos como fuente de
alimento.
6
Durante el
siglo XVIII comenzaron a surgir trabajos que relacionaban los incipientes conocimientos de la
Química con los de la
Biología. En la década de
1770, el
clérigo inglés Joseph Priestley (a quien se le atribuye el descubrimiento del O
2) estableció la producción de
oxígeno por los vegetales reconociendo que el proceso era, de forma aparente, el inverso de la
respiración animal, que consumía tal elemento químico. Fue Priestley quien acuñó la expresión de
aire deflogisticado
para referirse a aquel que contiene oxígeno y que proviene de los
procesos vegetales, así como también fue él quien descubrió la emisión
de dióxido de carbono por parte de las plantas durante los periodos de
penumbra, aunque en ningún momento logró interpretar estos resultados.
7
En el
año 1778, el
médico holandés Jan Ingenhousz dirigió numerosos experimentos dedicados al estudio de la producción de oxígeno por las plantas (muchas veces ayudándose de un
eudiómetro), mientras se encontraba de vacaciones en
Inglaterra,
para publicar al año siguiente todos aquellos hallazgos que había
realizado durante el transcurso de su investigación en el libro titulado
Experiments upon Vegetables.
Algunos de sus mayores logros fueron el descubrimiento de que las
plantas, al igual que sucedía con los animales, viciaban el aire tanto
en la luz como en la oscuridad; que cuando los vegetales eran iluminados
con luz solar, la liberación de aire cargado con oxígeno excedía al que
se consumía y la demostración que manifestaba que para que se produjese
el desprendimiento fotosintético de oxígeno se requería de luz solar.
También concluyó que la fotosíntesis no podía ser llevada a cabo en
cualquier parte de la planta, como en las raíces o en las flores, sino
que únicamente se realizaba en las partes verdes de ésta. Como médico
que era, Jan Ingenhousz aplicó sus nuevos conocimientos al campo de la
medicina y del bienestar humano, por lo que también recomendó sacar a
las plantas de las casas durante la noches para prevenir posibles
intoxicaciones.
8 6
En la misma línea de los autores anteriores,
Jean Senebier,
ginebrino,
realiza nuevos experimentos que establecen la necesidad de la luz para
que se produzca la asimilación de dióxido de carbono y el
desprendimiento de oxígeno. También establece, que aún en condiciones de
iluminación, si no se suministra CO
2, no se registra
desprendimiento de oxígeno. J. Senebier sin embargo opinaba, en contra
de las teorías desarrolladas y confirmadas más adelante, que la fuente
de dióxido de carbono para la planta provenía del agua y no del aire.
Otro autor suizo,
Nicolas-Théodore de Saussure, demostraría experimentalmente que el aumento de
biomasa
depende de la fijación de dióxido de carbono (que puede ser tomado
directamente del aire por las hojas) y del agua. También realiza
estudios sobre la
respiración en plantas y concluye que, junto con la emisión de dióxido de carbono, hay una pérdida de agua y una generación de
calor. Finalmente, de Saussure describe la necesidad de la nutrición
mineral de las plantas.
El químico alemán
Justus von Liebig, es uno de los grandes promotores tanto del conocimiento actual sobre
química orgánica, como sobre
fisiología vegetal,
imponiendo el punto de vista de los organismos como entidades
compuestas por productos químicos y la importancia de las reacciones
químicas en los procesos vitales. Confirma las teorías expuestas
previamente por de Saussure, matizando que si bien la fuente de carbono
procede del CO
2 atmosférico, el resto de los nutrientes proviene del
suelo.
La denominación como
clorofila de los pigmentos fotosintéticos fue acuñada por
Pelletier y
Caventou a comienzos del
siglo XIX.
Dutrochet, describe la entrada de CO
2 en la planta a través de los
estomas y determina que solo las células que contienen clorofila son productoras de oxígeno.
Hugo von Mohl, más tarde, asociaría la presencia de
almidón con la de clorofila y describiría la estructura de los estomas.
Sachs,
a su vez, relacionó la presencia de clorofila con cuerpos subcelulares
que se pueden alargar y dividir, así como que la formación de almidón
está asociada con la iluminación y que esta sustancia desaparece en
oscuridad o cuando los estomas son ocluidos. A Sachs se debe la
formulación de la ecuación básica de la fotosíntesis:
- 6 CO2 + 6 H2O → C6H12O6 + 6 O2
Andreas Franz Wilhelm Schimper daría el nombre de
cloroplastos a los cuerpos coloreados de Sachs y describiría los aspectos básicos de su estructura, tal como se podía detectar con
microscopía óptica.
En el último tercio del siglo XIX se sucederían los esfuerzos por
establecer las propiedades físico-químicas de las clorofilas y se
comienzan a estudiar los aspectos ecofisiológicos de la fotosíntesis.
Siglo XX
En
1905,
Frederick Frost Blackman
midió la velocidad a la que se produce la fotosíntesis en diferentes
condiciones. En un primer momento se centró en observar como variaba la
tasa de fotosíntesis modificando la intensidad lumínica, apreciando que
cuando la planta era sometida a una luz tenue cuya intensidad se iba
incrementando hasta convertirse en moderada, aumentaba la tasa
fotosintética, pero cuando se alcanzaban intensidades mayores no se
producía un aumento adicional. Con posterioridad investigó el efecto
combinado de la luz y de la temperatura sobre la fotosíntesis, de modo
que obtuvo los siguientes resultados: si bien, en condiciones de luz
tenue un aumento en la temperatura no tenía repercusión alguna sobre el
proceso fotosintético, cuando la intensidad luz y los grados aumentaban
la tasa de fotosíntesis si que experimentaba una variación positiva.
Finalmente, cuando la temperatura superaba los 30 °C, la fotosíntesis se
ralentizaba hasta que se sobrevenía el cesamiento del proceso.
A consecuencia de los resultados obtenidos, Blackman planteó que en
la fotosíntesis coexistían dos factores limitantes, que eran la
intensidad lumínica y la temperatura.
En la
década de 1920,
Cornelius Bernardus van Niel
propuso, tras haber estudiado a las bacterias fotosintéticas del
azufre, que el oxígeno liberado en la fotosíntesis provenía del agua y
no del dióxido de carbono, extrayéndose que el hidrógeno empleado para
la síntesis de
glucosa procedía de la
fotólisis del agua que había sido absorbida por la planta. Pero esta hipótesis no se confirmó hasta el
año 1941, tras las investigaciones realizadas por
Samuel Ruben y
Martin Kamen con agua con oxígeno pesado y una
alga verde (
Chlorella).
1 6
En
1937,
Robert Hill
logró demostrar que los cloroplastos son capaces de producir oxígeno en
ausencia de dióxido de carbono, siendo este descubrimiento uno de los
primeros indicios de que la fuente de electrones en las reacciones de la
fase clara de la fotosíntesis es el agua. Aunque cabe destacar que
Hill, en su experimento
in vitro empleó un
aceptor de electrones artificial. De estos estudios se derivó la conocida con nombre de
Reacción de Hill, definida como la fotoreducción de un aceptor artificial de electrones por los hidrógenos del agua, con liberación de oxígeno.
9
En la
década de 1940, el químico norteamericano
Melvin Calvin inició sus estudios e investigaciones sobre la fotosíntesis, que le valieron el
Premio Nobel de Química de
1961. Gracias a la aplicación del
carbono 14
radioactivo detectó la secuencia de reacciones químicas generadas por
las plantas al transformar dióxido de carbono gaseoso y agua en oxígeno e
hidratos de carbono, lo que en la actualidad se conoce como
ciclo de Calvin.
Un personaje clave en el estudio de la fotosíntesis fue el fisiólogo vegetal
Daniel Arnon. A pesar de que realizó descubrimientos botánicos de notable importancia (demostró que el
vanadio y el
molibdeno eran
micronutrientes
absorbidos por algas y plantas, respectivamente, y que intervenían en
el crecimiento de las mismas), es principalmente conocido por sus
trabajos orientados de cara a la fotosíntesis. Fue en
1954,
cuando sus colegas y él emplearon componentes de las hojas de las
espinacas para llevar a cabo la fotosíntesis en ausencia total de
células para explicar como éstas asimilan el dióxido de carbono y cómo forman ATP.
10 6
En el año
1982, los
químicos alemanes Johann Deisenhofer,
Hartmut Michel y
Robert Huber analizaron el centro de reacción fotosintético de las bacteria
Rhodopseudomonas viridis, y para determinar la estructura de los cristales del complejo proteico utilizaron la
cristalografía de rayos X.
Sin embargo, esta técnica resultó excesivamente compleja para estudiar
la proteína mencionada y Michel tuvo que idear un método espacial que
permitía la cristalografía de proteínas de membrana.
11 12 13 6
Cuando Michel consiguió las muestras cristalinas perfectas que
requería su análisis, su compañero de investigación desenvolvió los
métodos matemáticos para interpretan el patrón de
rayos X
obtenido. Aplicando estas ecuaciones, los químicos lograron identificar
la estructura completa del centro de reacción fotosintética, compuesto
por cuatro subunidades de proteínas y de 10.000 átomos. Por medio de
esta estructura, tuvieron la oportunidad con detalle del proceso de la
fotosíntesis, siendo la primera vez que se concretó la estructura
tridimensional de dicha proteína.
11 6
El cloroplasto
De todas las
células eucariotas, únicamente las fotosintéticas presentan cloroplastos, unos
orgánulos que usan la
energía solar para impulsar la formación de
ATP y
NADPH,
compuestos utilizados con posterioridad para el ensamblaje de azúcares y
otros compuestos orgánicos. Al igual que las mitocondrias, cuentan con
su propio
ADN y posiblemente se hayan originado como
bacterias simbióticas intracelulares (
Teoría endosimbiótica).
Desarrollo

Esquema ilustrativo de las clases de
plastos.
En las
células meristemáticas se encuentran
proplastos, que no tienen ni membrana interna, ni
clorofila, ni ciertos enzimas requeridos para llevar a cabo la fotosíntesis. En
angiospermas y
gimnospermas el desarrollo de los cloroplastos es desencadenado por la
luz, puesto que bajo iluminación se generan los enzimas en el interior del proplasto o se extraen del
citosol, aparecen los pigmentos encargados de la absorción lumínica y se producen con gran rapidez las membranas, dando lugar a los
grana y las
lamelas del
estroma.
14
A pesar de que las
semillas suelen
germinar
en el suelo sin luz, los cloroplastos son una clase de orgánulos que
exclusivamente se desarrollan cuando el vástago queda expuesto a la luz.
Si la semilla germina en ausencia de luz, los proplastos se diferencian
en etioplastos, que albergan una agrupación tubular semicristalina de
membrana llamada cuerpo prolamelar. En vez de
clorofila, estos
etioplastos tienen un pigmento de color verde-amarillento que constituye el precursor de la misma: es la denominada
protoclorofila.
14
Después de estar por un pequeño intervalo de tiempo expuestos a la
luz, los etioplastos se diferencian transformándose los cuerpos
prolamelares en
tilacoides y
lamelas del
estroma,
y la protoclorofila, en clorofila. El mantenimiento de la estructura de
los cloroplastos está directamente vinculada a la luz, de modo que si
en algún momento éstos pasan a estar en penumbra continuada puede
desencadenarse que los cloroplastos vuelvan a convertirse en
etioplastos.
14
Además, los cloroplastos pueden convertirse en
cromoplastos, como sucede en las hojas durante el
otoño o a lo largo del proceso de maduración de los frutos (proceso reversible en determinadas ocasiones). Asimismo, los
amiloplastos
(contenedores de almidón) pueden transformarse en cloroplastos, hecho
que explica el fenómeno por el cual las raíces adquieren tonos verdosos
al estar en contacto con la luz solar.
14
Estructura y abundancia
Se distinguen por ser unas estructuras polimorfas de
color verde,
siendo la coloración que presentan consecuencia directa de la presencia
del pigmento clorofila en su interior. Además, presentan una envoltura
formada por una doble membrana que carece de clorofila y
colesterol: una membrana plastidial externa y una membrana plastidial interna.
En las plantas superiores, la forma que con mayor frecuencia
presentan los cloroplastos es la de disco lenticular, aunque también
existen algunos de aspecto ovoidal o esférico. Con respecto a su número,
se puede decir que en torno a cuarenta y cincuenta cloroplastos
coexisten, de media, en una célula de una hoja; y existen unos 500.000
cloroplastos por milímetro cuadrado de superficie foliar. No sucede lo
mismo entre las algas, pues los cloroplastos de éstas no se encuentran
tan determinados ni en número ni en forma. Por ejemplo, en el alga
Spirogyra únicamente existen dos cloroplastos con forma de cinta en espiral, y en el alga
Chlamydomonas, sólo hay uno de grandes dimensiones.
En el interior y delimitado por una membrana plastidial interna, se
ubica una cámara que alberga un medio interno con un elevado número de
componentes (
ADN
plastidial, circular y de doble hélice, plastorribosomas, enzimas e
inclusiones de granos de almidón y las inclusiones lipídicas); es lo que
se conoce por el nombre de estroma. Inmerso en él se encuentran una
gran cantidad de sáculos denominados
tilacoides,
que contienen pigmentos fotosintéticos en su membrana tilacoidal (cuya
cavidad interior se llama lumen o espacio tilacoidal). Los tilacoides
pueden encontrarse repartidos por todo el estroma (tilacoides del
estroma), o bien, pueden ser pequeños, tener forma discoidal y
encontrarse apilados originando unos montones, denominados grana
(tilacoides de grana). Es en la
membrana
de los grana donde se ubican los sistemas enzimáticos encargados de
captar la energía lumínica, llevar a cabo el transporte de electrones y
sintetizar
ATP.
Función

Ecuación de la fotosíntesis oxigénica, función característica de los cloroplastos.
La más importante función realizada por los cloroplastos es la fotosíntesis, proceso en la que la
materia inorgánica es transformada en materia orgánica (fase oscura) empleando la energía bioquímica (
ATP) obtenida por medio de la energía solar, a través de los
pigmentos fotosintéticos y la cadena transportadora de
electrones
de los tilacoides (fase luminosa). Otras vías metabólicas de vital
importancia que se realizan en el estroma, son la biosíntesis de
proteínas y la replicación del
ADN.
Fase luminosa o fotoquímica
La energía lumínica que absorbe la clorofila se transmite a los
electrones externos de la molécula, los cuales escapan de la misma y
producen una especie de corriente eléctrica en el interior del
cloroplasto al incorporarse a la
cadena de transporte de electrones.
Esta energía puede ser empleada en la síntesis de ATP mediante la
fotofosforilación, y en la síntesis de NADPH. Ambos compuestos son
necesarios para la siguiente fase o Ciclo de Calvin, donde se
sintetizarán los primeros azúcares que servirán para la producción de
sacarosa y
almidón. Los electrones que ceden las clorofilas son repuestos mediante la oxidación del H
2O, proceso en el cual se genera el O
2 que las plantas liberan a la atmósfera.
Existen dos variantes de
fotofosforilación:
acíclica y cíclica, según el tránsito que sigan los electrones a través
de los fotosistemas. Las consecuencias de seguir un tipo u otro
estriban principalmente en la producción o no de NADPH y en la
liberación o no de O
2.
Fotofosforilación acíclica (oxigénica)
El proceso de la fase luminosa, supuesto para dos electrones, es el
siguiente: Los fotones inciden sobre el fotosistema II, excitando y
liberando dos electrones, que pasan al primer aceptor de electrones, la
feofitina. Los electrones los repone el primer dador de electrones, el
dador Z, con los electrones procedentes de la
fotólisis del agua en el interior del
tilacoide (la molécula de agua se divide en 2H
+ + 2e
- + 1/2O
2). Los
protones de la fotólisis se acumulan en el interior del tilacoide, y el oxígeno es liberado.
Los electrones pasan a una
cadena de transporte de electrones,
que invertirá su energía liberada en la síntesis de ATP. ¿Cómo? La
teoría quimioosmótica nos lo explica de la siguiente manera: los
electrones son cedidos a las
plastoquinonas, las cuales captan también dos protones del estroma. Los electrones y los protones pasan al complejo de
citocromos
bf, que bombea los protones al interior del tilacoide. Se consigue así
una gran concentración de protones en el tilacoide (entre éstos y los
resultantes de la fotólisis del agua), que se compensa regresando al
estroma a través de las proteínas
ATP-sintasas, que invierten la energía del paso de los protones en sintetizar ATP. La síntesis de ATP en la fase fotoquímica se denomina
fotofosforilación.
Los electrones de los citocromos pasan a la
plastocianina,
que los cede a su vez al fotosistema I. Con la energía de la luz, los
electrones son de nuevo liberados y captados por el aceptor A
0. De ahí pasan a través de una serie de
filoquinonas hasta llegar a la
ferredoxina. Ésta molécula los cede a la enzima
NADP+-reductasa, que capta también dos protones del estroma. Con los dos protones y los dos electrones, reduce un NADP
+ en NADPH + H
+.
El balance final es: por cada molécula de agua (y por cada cuatro
fotones) se forman media molécula de oxígeno, 1,3 moléculas de ATP, y un
NADPH + H
+.

Esquema de la etapa fotoquímica, que se produce en los tilacoides.
Fase luminosa cíclica (Fotofosforilación anoxigénica)
En la fase luminosa o fotoquímica cíclica interviene de forma
exclusiva el fotosistema I, generándose un flujo o ciclo de electrones
que en cada vuelta da lugar a síntesis de ATP. Al no intervenir el
fotosistema II, no hay fotólisis del agua y, por ende, no se produce la
reducción del NADP
+ ni se desprende oxígeno (anoxigénica). Únicamente se obtiene ATP.
El objetivo que tiene la fase cíclica tratada es el de subsanar el
déficit de ATP obtenido en la fase acíclica para poder afrontar la fase
oscura posterior.
Cuando se ilumina con luz de longitud de onda superior a 680 nm (lo que se llama
rojo lejano)
sólo se produce el proceso cíclico. Al incidir los fotones sobre el
fotosistema I, la clorofila P700 libera los electrones que llegan a la
ferredoxina, la cual los cede a un citocromo bf y éste a la plastoquinona (PQ), que capta dos protones y pasa a (PQH
2). La
plastoquinona
reducida cede los dos electrones al citocromo bf, seguidamente a la
plastocianina y de vuelta al fotosistema I. Este flujo de electrones
produce una diferencia de potencial en el tilacoide que hace que entren
protones al interior. Posteriormente saldrán al estroma por la
ATP-sintetasa fosforilando ADP en ATP. De forma que únicamente se
producirá ATP en esta fase.
Sirve para compensar el hecho de que en la fotofosforilación acíclica no se genera suficiente ATP para la fase oscura.
La fase luminosa cíclica puede producirse al mismo tiempo que la acíclica.
Fase oscura o biosintética
En la
fase oscura, que tiene lugar en la matriz o
estroma
de los cloroplastos, tanto la energía en forma de ATP como el NADPH que
se obtuvo en la fase fotoquímica se usa para sintetizar materia
orgánica por medio de sustancias inorgánicas. La fuente de carbono
empleada es el dióxido de carbono, mientras que como fuente de nitrógeno
se utilizan los nitratos y nitritos, y como fuente de azufre, los
sulfatos. Esta fase se llama oscura, no porque ocurra de noche, sino
porque no requiere de energía solar para poder concretarse.
- Síntesis de compuestos de carbono: descubierta por el
bioquímico norteamericano Melvin Calvin, por lo que también se conoce
con la denominación de Ciclo de Calvin, se produce mediante un proceso
de carácter cíclico en el que se pueden distinguir varios pasos o fases.
En primer lugar se produce la fijación del dióxido de carbono. En el
estroma del cloroplasto, el dióxido de carbono atmosférico se une a la
pentosa ribulosa-1,5-bisfosfato, gracias a la
enzima RuBisCO,
y origina un compuesto inestable de seis carbonos, que se descompone en
dos moléculas de ácido-3-fosfoglicérico. Se trata de moléculas
constituidas por tres átomos de carbono, por lo que las plantas que
siguen esta vía metabólica se llaman C3. Si bien, muchas especies
vegetales tropicales que crecen en zonas desérticas, modifican el ciclo
de tal manera que el primer producto fotosintético no es una molécula de
tres átomos de carbono, sino de cuatro (un ácido dicarboxílico),
constituyéndose un método alternativo denominado vía de la C4, al igual
que este tipo de plantas.
Con posterioridad se produce la reducción del dióxido de carbono
fijado. Por medio del consumo de ATP y del NADPH obtenidos en la fase
luminosa, el ácido 3-fosfoglicérico se reduce a gliceraldehído
3-fosfato. Éste puede seguir dos vías, consistiendo la primera de ellas
en regenerar la ribulosa 1-5-difosfato (la mayor parte del producto se
invierte en esto) o bien, servir para realizar otro tipo de biosíntesis:
el que se queda en el estroma del cloroplasto comienza la síntesis de
aminoácidos, ácidos grasos y almidón. El que pasa al citosol origina la
glucosa y la fructosa, que al combinarse generan la sacarosa (azúcar
característico de la savia) mediante un proceso parecido a la glucólisis
en sentido inverso.
La regeneración de la ribulosa-1,5-difosfato se lleva a cabo a partir
del gliceraldehído 3-fosfato, por medio de un proceso complejo donde se
suceden compuestos de cuatro, cinco y siete carbonos, semejante a ciclo
de las pentosas fosfato en sentido inverso (en el ciclo de Calvin, por
cada molécula de dióxido de carbono que se incorpora se requieren dos de
NADPH y tres de ATP).
- Síntesis de compuestos orgánicos nitrogenados: gracias al ATP
y al NADPH obtenidos en la fase luminosa, se puede llevar a cabo la
reducción de los iones nitrato que están disueltos en el suelo en tres
etapas.
En un primer momento, los iones nitrato se reducen a iones nitrito
por la enzima nitrato reductasa, requiriéndose el consumo de un NADPH.
Más tarde, los nitritos se reducen a amoníaco gracias, nuevamente, a la
enzima nitrato reductasa y volviéndose a gastar un NADPH. Finalmente, el
amoníaco que se ha obtenido y que es nocivo para la planta, es captado con rapidez por el ácido α-cetoglutárico originándose el
ácido glutámico
(reacción catalizada por la enzima glutamato sintetasa), a partir del
cual los átomos de nitrógeno pueden pasar en forma de grupo amino a
otros cetoácidos y producir nuevos aminoácidos.
Sin embargo, algunas bacterias pertenecientes a lo géneros
Azotobacter,
Clostridium y
Rhizobium y determinadas cianobacterias (
Anabaena y
Nostoc)
tienen la capacidad de aprovechar el nitrógeno atmosférico,
transformando las moléculas de este elemento químico en amoníaco
mediante el proceso llamada
fijación del nitrógeno. Es por ello por lo que estos organismos reciben el nombre de fijadores de nitrógeno.

Esquema en el que se muestra el proceso seguido en la síntesis de compuestos orgánicos nitrogenados.
- Síntesis de compuestos orgánicos con azufre: partiendo del
NADPH y del ATP de la fase luminosa, el ion sulfato es reducido a ion
sulfito, para finalmente volver a reducirse a sulfuro de hidrógeno. Este compuesto químico, cuando se combina con la acetilserina produce el aminoácido cisteína, pasando a formar parte de la materia orgánica celular.
Fotorrespiración
Este proceso, que implica el cierre de los estomas de las hojas como
medida preventiva ante la posible pérdida de agua, se sobreviene cuando
el ambiente es cálido y seco. Es entonces cuando el oxígeno generado en
el proceso fotosintético comienza a alcanzar altas concentraciones.
Cuando existe abundante dióxido de carbono, la enzima RuBisCO
(mediante su actividad como carboxilasa) introduce el compuesto químico
en el ciclo de Calvin con gran eficacia. Pero cuando la concentración de
dióxido de carbono en la hoja es considerablemente inferior en
comparación a la de oxígeno, la misma enzima es la encargada de
catalizar la reacción de la RuBisCO con el oxígeno (mediante su
actividad como oxigenasa), en lugar del dióxido de carbono. Esta
reacción es considerada la primera fase del proceso fotorrespiratorio,
en el que los glúcidos se oxidan a dióxido de carbono y agua en
presencia de luz. Además, este proceso supone una pérdida energética
notable al no generarse ni NADH ni ATP (principal rasgo que lo
diferencia de la respiración mitocondrial).
Cuando una molécula de RuBisCO reacciona con una de oxígeno, se
origina una molécula de ácido fosfoglicerico y otra de ácido
fosfoglicólico, que prontamente se hidroliza a ácido glicólico. Este
último sale de los cloroplastos para posteriormente introducirse en los
peroxisomas (orgánulos que albergan enzimas oxidativos), lugar en el que
vuelve a reaccionar con oxígeno para producir ácido glioxílico y
peróxido de hidrógeno (la acción de la enzima catalasa catalizará la
descomposición de este compuesto químico en oxígeno y agua). Sin embargo
el ácido glioxílico se transforma en glicina, aminoácido que se
traspasa a la mitocondrias para formarse una molécula de serina a partir
de dos de ácido glioxílico (este proceso conlleva la liberación de una
molécula de dióxido de carbono).
Ruta de Hatch-Slack o de las plantas C4
En los vegetales propias de las zonas con clima tropical, donde la
fotorrespiración podría revestir un problema de notable gravedad, se
presenta un proceso diferente para captar el dióxido de carbono. En
estas plantas se distinguen dos variedades de cloroplastos: existen unos
que se hallan en la células internas, contiguos a los vasos conductores
de las hojas, y otros que están en las células del parénquima
clorofílico periférico, lo que se llama mesófilo. Es en este último tipo
de cloroplasto en el que se produce la fijación del dióxido de carbono.
La molécula aceptora de este compuesto químico es el ácido
fosfoenolpirúvico (PEPA), y la enzima que actúa es la fosfoenolpiruvato
carboxilasa, que no se ve afectada por una alta concentración de
oxígeno.
Partiendo del ácido fosfoenolpirúvico y del dióxido de carbono se
genera el ácido oxalacético, constituido por cuatro carbonos (es de aquí
de donde proviene el nombre de plantas C4). El susodicho ácido se
transforma en málico, y este a través de los plasmodesmos, pasa a los
cloroplastos propios de las células internas. En estos se libera el
dióxido de carbono, que será apto para proseguir el ciclo de Calvin. A
consecuencia de ello, en estas plantas no se produce ningún tipo de
alteración a consecuencia de la respiración.
Las plantas CAM
La
sigla CAM es empleada como abreviación de la equívoca expresión inglesa
Crassulacean Acidic Metabolism,
que puede ser traducida al español como metabolismo ácido de las
Crasuláceas. Esta denominación se acuñó dado que en un principio este
mecanismo únicamente fue atribuido a las plantas pertenecientes a esta
familia, es decir, a las Crasuláceas. No obstante, en la actualidad se
conocen a varias especies de plantas CAM, que pertenecen a diferentes
familias de plantas crasas o suculentas (Crassulaceae, Cactaceae,
Euphorbiaceae, Aizoaceae son tan sólo algunos ejemplos). Por norma
general, las plantas CAM son vegetales originarios de zonas con unas
condiciones climáticas desérticas o subdesérticas, que se encuentran
sometidas a una intensa iluminación, a altas temperaturas y a un déficit
hídrico permanente. Pueden ser enumeradas muchas peculiaridades de
estas plantas, como que el tejido fotosintético es homogéneo, siendo
apreciable además la inexistencia de vaina diferenciada y de clorénquima
en empalizada.
5
Como ha sido mencionado, las plantas CAM se encuentra perfectamente
adaptadas a las condiciones de aridez extremas, por lo que resulta
lógico que sus estomas se abran durante la noche, para evitar en la
medida de lo posible la pérdida de agua por transpiración, fijando
dióxido de carbono en oscuridad por una reacción de carboxilación de PEP
(
ácido fosfoenolpirúvico)
catalizada por PEP carboxilasa en el citosol. Como resultado se produce
la formación de oxalacetato y malato que es almacenado en la vacuola,
sobreviniéndose una acidificación nocturna de la hoja. El malato
almacenado en la vacuola es liberado durante el día mientras los estomas
permanecen cerrados, siendo llevado al cloroplasto. Una vez en el
orgánulo mentado, el malato es descarboxilado por la enzima málico NADP
dependiente y el dióxido de carbono que se desprende es fijado en el
ciclo de Calvin. El ácido pirúvico se convierte nuevamente en azúcares,
para finalmente convertirse en almidón. La fijación y reducción del
carbono en las plantas CAM presenta unos requerimientos energéticos, en
términos de ATP, mayores que en las plantas C3 y C4; su rendimiento
fotosintético por unidad de tiempo es menor y su crecimiento es más
lento. Como consecuencia de la adaptación de estas plantas a sus
hábitats extremos, los mecanismos que regulan el equilibrio entre
transpiración y fotosíntesis están encaminados fuertemente hacia la
minimización de las pérdidas de agua, asegurando así la supervivencia en
el medio desértico, aunque a costa de una menor productividad.
5
También se tiene constancia de la existencia de plantas que poseen la
capacidad de adaptar su metabolismo a las condiciones ambientales de
modo que pueden presentar un ciclo CAM de carácter adaptativo, es decir,
aunque se comportan como C3 pueden inducir el ciclo CAM cuando están
sometidas a ciertas circunstancias. Son las denominadas CAM
facultativas, siendo ejemplo representativo de ellas la
Mesembryanthemum crystallinum, la cual realiza ciclo C3 en condiciones normales de no estrés, pero cambia a ciclo CAM en respuesta a situaciones de estrés.
5
Fotosistemas y pigmentos fotosintéticos
Los fotosistemas
Los pigmentos fotosintéticos se hallan alojados en unas proteínas
transmembranales que forman unos conjuntos denominados fotosistemas, en
los que se distinguen dos unidades diferentes: la antena y el centro de
reacción.
En la antena, que también puede aparecer nombrada como
LHC (abreviatura del
inglés Light Harvesting Complex),
predominan los pigmentos fotosintéticos sobre las proteínas. De hecho,
existen entre doscientas y cuatrocientas moléculas de pigmentos de
antena de varios tipos y tan sólo dos proteínas intermembranales. Sin
embargo, la antena carece de pigmento diana.
En el centro de reacción, mentado en algunas ocasiones como
CC (abreviatura del inglés
Core Complex),
las proteínas predominan sobre los pigmentos. En el centro de reacción
es donde está el pigmento diana, el primer aceptor de electrones y el
primer dador de electrones. En término generales, se puede decir que
existe una molécula de pigmento diana, unas cuantas de pigmentos no
diana, una de primer dador de electrones y una de primer aceptor.
Mientras existen entre dos y cuatro proteínas de membrana.
Fotosistema I y Fotosistema II
- El Fotosistema I (PSI) capta la luz cuya longitud de onda es menor o
igual a 700 nm y en las plantas superiores, su antena se caracteriza
por encerrar dentro de sí una gran proporción de clorofila α, y una
menor de clorofila β. En el centro de reacción, la molécula diana es la
clorofila αI que absorbe a 700 nm, siendo llamada por ello clorofila P700. El aceptor primario de electrones se denomina aceptor A0 y el dador primario es la plastocianina. Sobre todo, se hallan presentes en los tilacoides del estroma.
- El Fotosistema II (PSII) capta luz cuya longitud de onda es menor o igual a 680nm.
Los pigmentos fotosintéticos y la absorción de la luz
Los pigmentos fotosintéticos son
lípidos que se hayan unidos a
proteínas presentes en algunas
membranas plasmáticas,
y que se caracterizan por presentar alternancia de enlaces sencillos
con enlaces dobles. Esto se relaciona con su capacidad de
aprovechamiento de la
luz para iniciar reacciones químicas, y con poseer color propio. En las plantas se encuentran las
clorofilas y los
carotenoides; en las
cianobacterias y las
algas rojas también existe ficocianina y ficoeritrina; y finalmente, en las
bacterias fotosintéticas está la
bacterioclorofila.
La clorofila está formada por un anillo porfirínico con un
átomo de
magnesio en el centro, asociado a un
metanol y a un fitol (monoalcohol de compuesto de veinte
carbonos). Como consecuencia, se conforma una
molécula de carácter
anfipático, en donde la porfirina actúa como polo
hidrófilo y el fitol como polo
lipófilo. Se distinguen dos variedades de clorofila: la
clorofila a, que alberga un
grupo metilo en el tercer carbono porfirínico y que absorbe luz de
longitud de onda cercana a 630
nm, y la
clorofila b, que contiene un grupo formilo y que absorbe a 660 nm.
Los
carotenoides son
isoprenoides y absorben luz de 440 nm, pudiendo ser de dos clases: los
carotenos, que son de color rojo, y las
xantófilas,
derivados oxigenados de los nombrados anteriormente, que son de color
amarillento. Las ficocianinas y las ficoeritrinas, de color azul y rojo
respectivamente, son lípidos que se hayan asociados a proteínas
originando las ficobiliproteínas.
Como los pigmentos fotosintéticos tienen
enlaces covalentes
sencillos que se alternan con enlaces covalentes dobles, se favorece la
existencia de electrones libres que no pueden atribuirse a un átomo
concreto.
Cuando incide un
fotón sobre un
electrón de un pigmento fotosintético de antena, el electrón capta la
energía del fotón y asciende a posiciones más alejadas del
núcleo atómico.
En el supuesto caso de que el pigmento estuviese aislado, al descender
al nivel inicial, la energía captada se liberaría en forma de
calor o de
radiación de mayor longitud de onda (
fluorescencia).
Sin embargo, al existir diversos tipos de pigmentos muy próximos, la
energía de excitación captada por un determinado pigmento puede ser
transferida a otro al que se induce el estado de excitación. Este
fenómeno se produce gracias a un estado de resonancia entre la molécula
dadora relajada y la aceptora. Para ello se necesita que el espectro de
emisión del primero coincida, al menos en parte, con el de absorción del
segundo. Los
excitones
se transfieren siempre hacia los pigmentos que absorben a mayor
longitud de onda, continuando el proceso hasta alcanzar el pigmento
fotosintético diana.
Factores externos que influyen en el proceso
Mediante la comprobación experimental, los científicos han llegado a la conclusión de que la
temperatura, la
concentración de determinados
gases en el aire (tales como
dióxido de carbono y
oxígeno), la
intensidad luminosa y la
escasez de
agua son aquellos factores que intervienen aumentando o disminuyendo el rendimiento fotosintético de un vegetal.
- La temperatura: cada especie se encuentra adaptada a vivir en
un intervalo de temperaturas. Dentro de él, la eficacia del proceso
oscila de tal manera que aumenta con la temperatura, como consecuencia
de un aumento en la movilidad de las moléculas, en la fase oscura, hasta llegar a una temperatura en la que se sobreviene la desnaturalización enzimática, y con ello la disminución del rendimiento fotosintético.15 16
- La concentración de dióxido de carbono: si la intensidad luminosa es alta y constante, el rendimiento fotosintético aumenta en relación directa con la concentración de dióxido de carbono en el aire, hasta alcanzar un determinado valor a partir del cual el rendimiento se estabiliza.15 16
- La concentración de oxígeno: cuanto mayor es la concentración
de oxígeno en el aire, menor es el rendimiento fotosintético, debido a
los procesos de fotorrespiración.15
- La intensidad luminosa: cada especie se encuentra adaptada a
desarrollar su vida dentro de un intervalo de intensidad de luz, por lo
que existirán especies de penumbra y especies fotófilas. Dentro de cada
intervalo, a mayor intensidad luminosa, mayor rendimiento, hasta
sobrepasar ciertos límites, en los que se sobreviene la fotooxidación
irreversible de los pigmentos fotosintéticos. Para una igual intensidad
luminosa, las plantas C4 (adaptadas a climas secos y cálidos)
manifiestan un mayor rendimiento que las plantas C3, y nunca alcanzan la
saturación lumínica.15 16
- El tiempo de iluminación: existen especies
que desenvuelven una mayor producción fotosintética cuanto mayor sea el
número de horas de luz, mientras que también hay otras que necesitan
alternar horas de iluminación con horas de oscuridad.17 16
- La escasez de agua: ante la falta de agua en el terreno y de vapor de agua
en el aire disminuye el rendimiento fotosintético. Esto se debe a que
la planta reacciona, ante la escasez de agua, cerrando los estomas para evitar su desecación,
dificultando de este modo la penetración de dióxido de carbono. Además,
el incremento de la concentración de oxígeno interno desencadena la
fotorrespiración. Este fenómeno explica que en condiciones de ausencia
de agua, las plantas C4 sean más eficaces que las C3.15 16
- El color de la luz: la clorofila α y la clorofila β absorben la energía lumínica en la región azul y roja del espectro,
los carotenos y xantofilas en la azul, las ficocianinas en la naranja y
las ficoeritrinas en la verde. Estos pigmentos traspasan la energía a
las moléculas diana. La luz monocromática menos aprovechable en los
organismos que no tienen ficoeritrinas y ficocianinas es la luz. En las cianofíceas,
que si poseen estos pigmentos anteriormente citados, la luz roja
estimula la síntesis de ficocianina, mientras que la verde favorece la
síntesis de ficoeritrina. En el caso de que la longitud de onda superase
los 680 nm, no actúa el fotosistema II con la consecuente reducción del
rendimiento fotosintético al existir únicamente la fase luminosa
cíclica.17
Fotosíntesis anoxigénica o bacteriana
Las bacterias únicamente son poseedoras de fotosistemas I, de manera
que al carecer de fotosistemas II no están capacitadas para usar al agua
como dador de electrones (no hay fotólisis del agua), y en
consecuencia, no producen oxígeno al realizar la fotosíntesis. En
función de la molécula que emplean como dador de electrones y el lugar
en el que acumulan sus productos, es posible diferenciar tres tipos de
bacterias fotosintéticas: las sulfobacterias purpúreas se caracterizan
por emplear
sulfuro de hidrógeno (
H2S)
como dador de electrones y por acumular el azufre en gránulos de azufre
en su interior; las sulfobacterias verdes también utilizan al sulfuro
de hidrógeno, pero a diferencia de las purpúreas no acumulan azufre en
su interior; y finalmente, las bacterias verdes carentes de azufre usan
materia orgánica, tal como ácido láctico, como donadora de electrones.
En las bacterias purpúreas, los fotosistemas I están presentes en la
membrana plasmática, mientras que en las bacterias verdes, estos se
encuentran en la membrana de ciertos orgánulos especiales. Los pigmentos
fotosintéticos están constituidos por las
bacterioclorofilas a,
b,
c,
d y
e, así como también por los carotenos; por otra parte, lo más frecuente es que la molécula diana sea la denominada P890.
Al igual que sucede en la fotosíntesis oxigénica, existe tanto una
fase dependiente de luz como una independiente de luz, distinguiéndose
en la primera un transporte de electrones acíclico y otro cíclico.
Mientras en el cíclico únicamente se obtiene ATP, en el acíclico se
reduce el NAD
+ a NADH, que posteriormente es empleado para la reducción del CO
2 , NO
3-, entre otros. El NADH también puede ser obtenido en ausenca de luz, gracias al ATP procedente del proceso cíclico.
Fotosíntesis artificial
Actualmente, existe un gran número de proyectos químicos destinados a
la reproducción artificial de la fotosíntesis, con la intención de
poder capturar
energía solar
a gran escala en un futuro no muy lejano. A pesar de que todavía no se
ha conseguido sintetizar una molécula artificial capaz de perdurar
polarizada
durante el tiempo necesario para reaccionar de forma útil con otra
moléculas, las perspectivas son prometedoras y los científicos son
optimistas.
18
Intentos de imitación de las estructura fotosintéticas
Desde hace cuatro décadas, en el ambiente científico se ha extendido
el interés por la creación de sistemas artificiales que imiten a la
fotosíntesis. Con frecuencia, lo que se hace es reemplazar a la
clorofila por una amalgama de compuestos químicos, ya sean orgánicos o
inorgánicos, que tienen la capacidad de captar la luz. Sin embargo, se
desconoce lo que se debe de hacer con los electrones liberados en el
proceso fotosintético.
19
En el
año 1981 fue fabricado el primer cloroplasto de carácter artificial,
20
que se encontraba constituido por una mezcla de compuestos orgánicos
sintéticos relacionados con la clorofila y que, al iluminarse, tenía la
capacidad de llevar a cabo la reacción de fotólisis del agua, generando
hidrógeno y oxígeno en estado gas. El tamaño físico del cloroplasto
artificial era mucho mayor en comparación con el de los cloroplastos
naturales, y además, su eficacia de conversión de energía lumínica en
química era notablemente inferior. Este primer experimento fue todo un
hito y supuso el primer paso hacia la construcción de un dispositivo
fotosintético obtenido artificialmente que funcionara.
19
En
1998, el equipo de
Thomas Moore,
profesor de química del Centro de Bioenergía y Fotosíntesis de la
Universidad Estatal de Arizona, decidió incorporar al cloroplasto artificial desarrollado años antes, una
vesícula
rodeada de una cubierta parecida a las membranas de los cloroplastos
naturales. En ella se hallaban las clorofilas tratadas sintéticamente,
junto con otros compuestos que se añadieron con la intención de generar
una acumulación de iones
H+ en la parte interna de la membrana. Pero el hecho más destacable del experimento fue la incorporación de la
enzima ATP-sintetasa, principal responsable del aprovechamiento del desequilibrio en la concentración de
H+
para producir ATP. Con estas modificaciones, Moore consiguió un
comportamiento similar al de los cloroplastos reales, sintetizando ATP a
partir de energía solar, pero con un número más reducido de componentes
que la cadena fotosintética natural. Tal fue la repercusión del
experimento, que en la actualidad se continúan explorando sus
aplicaciones prácticas.
19
En
1999, científicos
norteamericanos
unieron químicamente cuatro moléculas de clorofila, dando lugar a una
cadena por la que podían circular los electrones y en cuyo remate, se
encontraba una bola de
fullereno C60. Tras incidir la luz en el sistema, los electrones emitidos eran trasportados hasta la bola de
buckminsterfullereno
que se quedaba cargada eléctricamente y mantenía estable su carga. Pero
el principal defecto de este imaginativo proyecto es que los
científicos que lo lideraban desconocían la posible aplicación del
fullereno cargado que se había obtenido por medio del proceso
mencionado.
19
Célula de Grätzel
Las células de Grätzel son
dispositivos fotovoltaicos de
dióxido de titanio nanoestructurado
sensitivizado con colorante, cuyos mecanismos para la transferencia
electrónica se caracterizan por ser parecidos a los que se producen en
la planta durante el proceso fotosintético. De hecho, el colorante, que
puede ser de naturaleza sintética o natural, permite el empleo de la
clorofila para este tipo de dispositivos.
A pesar de que ya en
1972,
el alemán Helmunt Tributsch había creado células solares
fotoelectroquímicas sensitivizadas con colorante, con capacidad para
producir electricidad, usando electrodos densos convencionales. Los
desarrollos con electrodos de óxidos sensitivizados generaron
eficiencias próximas al 2,5% limitadas por la reducida superficie
fotoactiva de estos electrodos.
La principal traba de este proyecto es su
eficiencia,
que se sitúa en torno al 11% en un laboratorio, pero si se extrapola a
un nivel industrial disminuye de forma notoria. Es por ello por lo que
investigadores de todo el mundo (algunos ejemplos son el grupo de
trabajo encabezado por el Michael Grätzel en
Lausanne o los científicos de la
Universidad Pablo de Olavide) trabajan para incrementar la eficiencia, así como para descubrir configuraciones alternativas y más prácticas.
A pesar de que su introducción en el mercado es todavía muy limitada, ya existen empresas como la
australiana Sustainable Technologies International que en el
año 2001,
y tras un programa de desarrollo que alcanzó el coste de doce millones
de dólares, implantó de forma pionera una planta de producción a gran
escala de células solares de titanio sensitivizado.
Disoluciones homogéneas
El
31 de agosto del
2001 se publicó el la
revista Science, un artículo en el que se recogía el resultado de un experimento realizado por unos investigadores del
Instituto Tecnológico de Massachussets,
consistente en obtener hidrógeno por medio de disoluciones de ácido
clorhídrico, usando como catalizador un compuesto orgánico de naturaleza
sintética contenedor de átomos de
rodio como centro activo.
19
El hecho de que la regeneración del catalizador de rodio no sea
perfecta, obliga a tener que reabastecerlo cada cierto período para
mantener la reacción, por lo que en la actualidad se sigue investigando
para obtener el catalizador que mejor se adecue.
19
Véase también
Referencias
- ↑ Saltar a: a b c Universidad Politécnica de Valencia. «La Fotosíntesis». Consultado el 5 de diciembre de 2009.
- Ir a ↑ Field CB, Behrenfeld MJ, Randerson JT, Falkowski P (1998). «Primary production of the biosphere: integrating terrestrial and oceanic components». Science 281. 237 - 240.
- Ir a ↑ Antonio Jimeno, Manuel Ballesteros, Luis Ugedo (2003). Biología (2º de Bachillerato). Santillana. pp. 210. ISBN 978-84-294-8385-7.
- Ir a ↑ Agencia EFE. «La vida en la Tierra surgió 800 millones de años antes de lo que se pensaba». Consultado el 27 de noviembre de 2009.
- ↑ Saltar a: a b c d Elena Pérez-Urria Carril (Facultad de Ciencias Biológicas de la Universidad Complutense de Madrid). «Fotosíntesis: Aspectos Básicos». Consultado el 27 de noviembre de 2009.
- ↑ Saltar a: a b c d e f Universidad Nacional de Colombia. «Fisiología vegetal (descubrimientos importantes para la teoría fotosintética)». Consultado el 24 de noviembre de 2009.
- Ir a ↑ Frank Bradley Armstrong (1982). Bioquímica. Reverté. pp. 320. ISBN 84-291-7008-1.
- Ir a ↑ Duane Isely (2002). One Hundred and One Botanists. pp. 104, 105 y 106. ISBN 1-55753-283-4.
- Ir a ↑ Universidad de Las Américas. Instituto de Ciencias Naturales (Laboratorio de Fisiología Vegetal). «Fotosíntesis (1. Reacción de Hill)». Consultado el 29 de noviembre de 2009.
- Ir a ↑ Biblioteca Premium Microsoft Encarta 2006, Daniel Arnon
- ↑ Saltar a: a b Biblioteca Premium Microsoft Encarta 2006, Johann Deisenhofer
- Ir a ↑ Biblioteca Premium Microsoft Encarta 2006, Hartmut Michel
- Ir a ↑ Biblioteca Premium Microsoft Encarta 2006, Robert Huber
- ↑ Saltar a: a b c d Eduardo Zeiger, Lincoln Taiz (2006). Fisiología Vegetal. Publicacions de la Universitat Jaume I. pp. 26, 27. ISBN 978-84-8021-601-2.
- ↑ Saltar a: a b c d e Antonio Jimeno, Manuel Ballesteros, Luis Ugedo (2003). Biología (2º de Bachillerato). Santillana. pp. 220. ISBN 978-84-294-8385-7.
- ↑ Saltar a: a b c d e Puigdomènech, Pedro (1986). Enciclopedia de las Ciencias; Las plantas, el mundo de la botánica. Ediciones Orbis S.A. pp. 19. ISBN 978-84-294-8385-7.
- ↑ Saltar a: a b Antonio Jimeno, Manuel Ballesteros, Luis Ugedo (2003). Biología (2º de Bachillerato). Santillana. pp. 221. ISBN 978-84-294-8385-7.
- Ir a ↑ Biblioteca Premium Microsoft Encarta 2006, Fotosíntesis (apartado Fotosíntesis Artificial)
- ↑ Saltar a: a b c d e f Owen Wangensteen. «Fotosíntesis Artificial (Apartado de Ingeniería)». Consultado el 31 de diciembre de 2009.
- Ir a ↑ Magdalena Rius de Riepen, Carlos Mauricio Castro-Acuña (1989). La química hacia la conquista del Sol. pp. 77. ISBN 968-16-6615-1.
Bibliografía básica
- J. Azcón-Bieto, M. Talón (eds.). Fundamentos de Fisiología Vegetal.
Madrid: McGraw-Hill/Interamericana, Edicions Universitat de Barcelona,
2000.
- B.B. Buchanan, W. Gruissem, R. Jones. Biochemistry and Molecular
Biology of plants. Rockville (USA): American Society of Plant
Physiologists, 2000.
- D. T. Dennis and D.H. Turpin (eds). Plant metabolism. Plant
physiology, Biochemistry, and Molecular Biology. Orlando, USA: Academic
Press, 1998.
- H.W. Heldt. Plant Biochemistry and Molecular Biology. Oxford (U.K.): Oxford University Press, 2004.
- Frank B. Salisbury, Cleon W. Ross. Fisiología Vegetal. México: Grupo
Editorial Iberoamericana, 1994. (traducción de la 4ª edición original
en inglés: Plant Physiology. Wadsworth, 1992; existe también una
reedición de la versión española en tres volúmenes: Madrid: Paraninfo,
2000).
- L. Taiz, E. Zeiger. Plant Physiology. Sunderland, Massachussets: Sinauer Associates Inc., 2002.
Enlaces externos